синдром распада опухоли код по мкб 10
Синдром распада опухоли
Рубрика МКБ-10: E88.3
Содержание
Определение и общие сведения [ править ]
Cиндром распада опухоли
Синонимы: Тумор-лизис синдром (ТЛС), синдрома лизиса опухоли
Синдром быстрого распада опухоли (СБРО) возникает при быстрой гибели большой массы опухолевых клеток.
Этиология и патогенез [ править ]
Чаще всего синдром быстрого распада опухоли наблюдают в начале цитостатической терапии у больных:
• с острыми и хроническими лимфобластными лейкозами и лимфомами (лимфома Беркита);
• при других опухолях, чувствительных к химиотерапевтическому, биотерапевтическому и лучевому лечению;
• иногда синдром быстрого распада опухоли развивается спонтанно, ещё до начала противоопухолевого лечения (лимфома Беркита).
Клинические проявления [ править ]
Симптомы синдрома быстрого распада опухоли варьируют.
• Кратковременные тонические судороги и сонливость, обусловленные гиперфосфатемией и вторичной гипокальциемией.
• ОПН связана с гиперурикемией (мочекислая или уратная нефропатия) и/или гиперфосфатемией (фосфатная нефропатия). В обоих случаях первично поражены почечные канальцы. Риск развития ОПН повышен у больных с предшествующим нарушением функции почек (нефротоксичная химиотерапия, ХПН любой этиологии) и/или не корригированными до начала химиотерапии метаболическим ацидозом и дегидратацией.
• Тяжёлая дыхательная недостаточность.
• Остановка сердечной деятельности вследствие фатальной аритмии или гиперкалиемии.
Синдром распада опухоли: Диагностика [ править ]
Дифференциальный диагноз [ править ]
Синдром распада опухоли: Лечение [ править ]
Лечение синдрома быстрого распада опухоли заключается в энергичной гидратации и коррекции электролитных нарушений, для чего применяют гидроксид алюминия, диуретики, ГФ и другие методы лечения.
• Гидроксид алюминия применяют внутрь для связывания фосфатов.
• Консервативное лечение гиперкалиемии заключается в поддержании высокого диуреза, гидратации и коррекции негазового ацидоза.
Профилактика [ править ]
• Гидратацию изотоническими или гипотоническими жидкостями (0,9% раствор хлорида натрия, раствор Рингера) в суточном объёме 3000 мл/м2 (200-250 мл/ч) начинают за несколько часов до введения цитостатиков. Обычно в ответ на водно-солевую нагрузку диурез увеличивается, и через 2-4 ч темп диуреза равен темпу инфузии.
• При выраженной задержке жидкости применяют низкие дозы петлевых диуретиков (фуросемид) или ацетазоламид в дозе 5 мг/кг в сутки.
• Предотвратить развитие уратной нефропатии можно, поддерживая щелочную реакцию мочи (pH >7) внутривенным введением гидрокарбоната натрия (обычно в дозе 100-150 мэкв на каждый литр инфузионных растворов). Однако щелочная реакция мочи способствует образованию в канальцах нерастворимой соли (фосфата кальция), поэтому после начала химиотерапии введение гидрокарбоната натрия следует ограничить только случаями декомпенсированного негазового ацидоза.
• Аллопуринол ингибирует фермент ксантиноксидазу и препятствует превращению ксантина в мочевую кислоту, назначают препарат до начала цитостатической терапии (при возможности, за 1-2 дня); приём аллопуринола следует продолжать и после проведения химиотерапии вплоть до нормализации уровня мочевой кислоты (по 500 мг/м2 в сутки за 1-2 дня до и в первые 3 дня химиотерапии, в последующие дни по 200 мг/м2 в сутки). В редких случаях (при почечной недостаточности) применение аллопуринола осложняется развитием гиперксантинурии и ксантиновой нефропатии. Ксантин растворим втрое меньше, чем мочевая кислота, и преципитирует даже при щелочной реакции мочи.
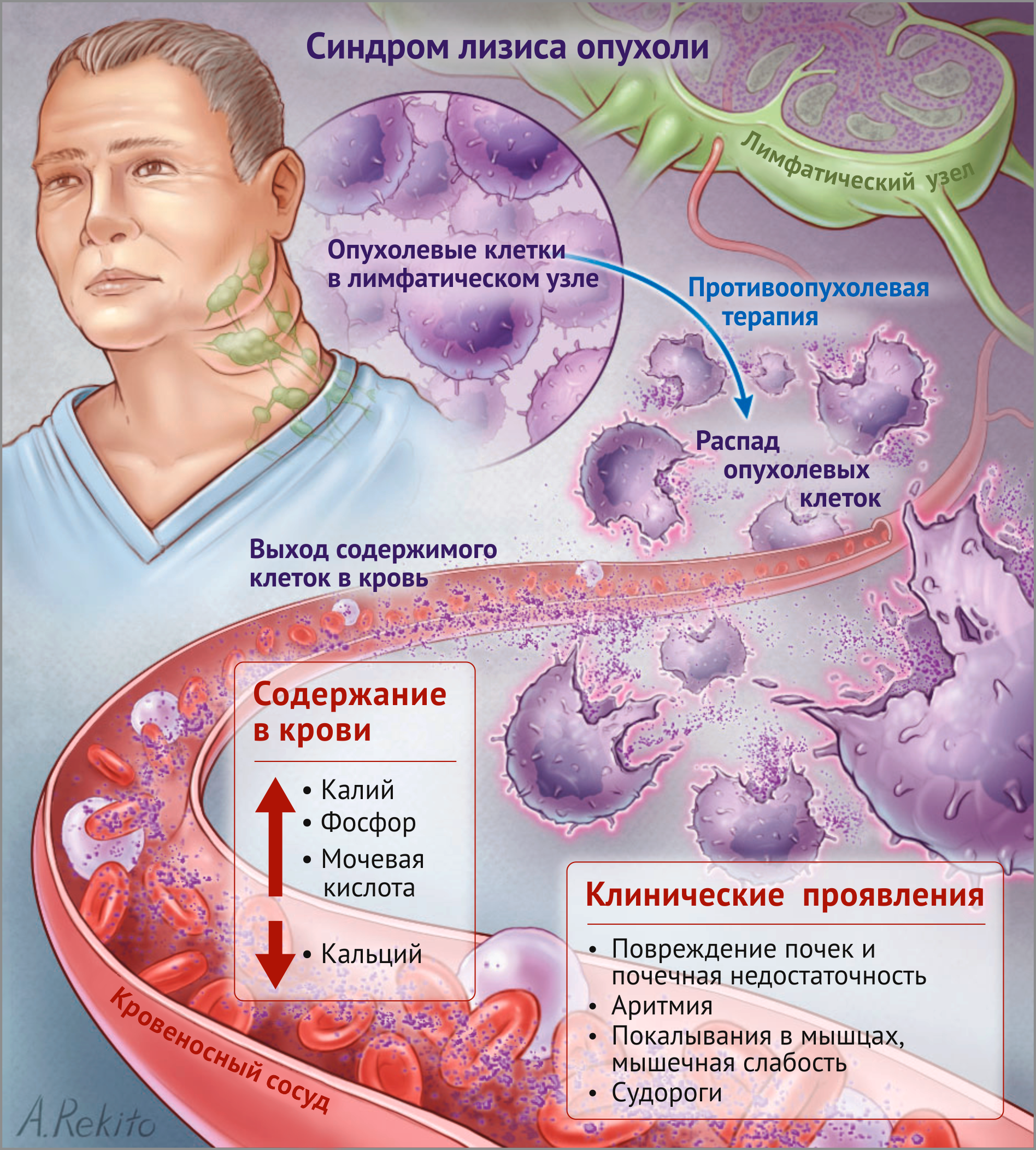
Синдром лизиса опухоли
Синдром распада опухоли (СРО) — это состояние, которое развивается при распаде большого количества опухолевых клеток за короткий период времени с высвобождением клеточного содержимого в кровь.
Как СРО влияет на организм?
При быстром распаде клеток опухоли концентрации мочевой кислоты, калия и фосфора в крови возрастают быстрее, чем почки могут удалить данные вещества. Это вызывает СРО. Избыточный фосфор способен «удерживать» кальций, что снижает его уровень в крови. Изменения концентрации мочевой кислоты, калия, фосфора и кальция в крови могут влиять на работу внутренних органов: сердца, головного мозга, мышц, желудочно-кишечного тракта и особенно почек.
Что способствует СРО?
Не у всех онкобольных одинаковый риск развития СРО. Он встречается чаще у пациентов с массивными опухолями и/или опухолями, которые могут характеризоваться очень высокой скоростью деления клеток, например, такими как острая лейкемия или высокодифференцированная лимфома. Еще один фактор риска СРО — хороший ответ опухоли на терапию. СРО может возникать спонтанно (до начала терапии), однако чаще всего данный синдром инициируется в течение первой недели после начала лечения. СРО не ограничивается пациентами, получающими традиционную химиотерапию: он может также возникать у тех, кто принимает стероиды, гормоны, таргетную или лучевую терапию. Обезвоженные пациенты с уже существующей почечной дисфункцией находятся в группе высокого риска возникновения СРО.
Каковы симптомы СРО и как его диагностировать?
Как правило, симптомы не являются специфичными. К ним относятся:
Диагностика СРО основывается на сопоставлении результатов анализа крови и симптомов. Его начало может быть подострым, при этом заподозрить развитие синдрома можно лишь по нескольким лабораторным отклонениям, однако данное состояние может также дебютировать с явной клинической картиной почечной и полиорганной недостаточности.
Можно ли предотвратить СРО?
Некоторые меры могут снизить шансы развития СРО. Лечащему врачу стоит тщательно изучить результаты анализов крови и характеристики опухоли, чтобы определить риск развития СРО у пациента и оценить, какие профилактические меры можно использовать. Внутривенные вливания могут помочь почкам вымыть токсины в мочу. Для снижения уровня мочевой кислоты могут быть назначены такие препараты, как Аллопуринол и Расбуриказа.
Как лечить СРО?
Даже с применением превентивных мер сохраняется риск развития СРО. Пациенты с высоким риском СРО должны находиться под более тщательным лабораторным и клиническим мониторингом до и во время терапии, чтобы обеспечить раннюю диагностику СРО, если он начнет развиваться. Лечение аналогично профилактическим мерам, включая внутривенные вливания, Аллопуринол и особенно Расбуриказу. Пациентам может потребоваться перенаправление в отделение интенсивной терапии. Анализы крови и мочи, оценка сердечного ритма — должны повторяться часто, чтобы оценить уровни электролитов и маркеров повреждения почек. Необходима тщательная коррекция электролитных нарушений. Некоторым пациентам с тяжелыми повреждениями почек может временно потребоваться гемодиализ.
Внеорганные забрюшинные опухоли
Общая информация
Краткое описание
Внеорганные забрюшинные опухоли – группа злокачественных и доброкачественных новообразований мезодермального, нейрогенного и эмбриогенного происхождения, локализующихся в забрюшинном пространстве.
Код(ы) МКБ-10:
| МКБ-10 | |
| Код | Название |
| C 48 | Внеорганные забрюшинные опухоли |
| в/в | внутривенно |
| в/м | внутримышечно |
| п/к | подкожно |
| per os | перорально |
| АлаТ | аланинаминотрансфераза |
| АПТВ | активированное парциальное тромбопластиновое время |
| АсаТ | аспартатаминотрансфераза |
| АЧТВ | активированное частичное тромбопластиновое время |
| ВИЧ | вирус иммунодефицита человека |
| ГИСО | гастроинтестинальные стромальные опухоли |
| Гр | грей |
| ЗНО | злокачественное новообразование |
| ИГХ | иммуногистохимическое исслед ование |
| ИФА | иммуноферментный анализ |
| КТ | компьютерная томография |
| МНН | международное непатентованное название |
| МРТ | магнитно-резонансная томография |
| НЭО | нейроэндокринные опухоли |
| ОАК | общий анализ крови |
| ОАМ | общий анализ мочи |
| ПМСП | первичная медико-санитарная помощь |
| ПТИ | протромбиновый индекс |
| ПЦР | полимеразная цепная реакция |
| ПЭТ | позитронно-эмиссионная томография |
| РОД | разовая очаговая доза |
| РОД | разовая очаговая доза |
| РЭА | раковоэмбриональный антиген |
| СЗП | свежезамороженная плазма |
| СОД | суммарная очаговая доза |
| ССС | сердечно-сосудистая система |
| УЗДГ | ультразвуковое допплерография |
| УЗИ | ультразвуковое исследование |
| ФЭГДС | фиброэзофагогастродуоденоскопия |
| ЭКГ | электрокардиограмма |
| ЭхоКГ | эхокардиография |
| TNM Tumor Nodulus Metastasis | международная классификация стадий злокачественных новообразований |
Дата разработки протокола: 2017 год.
Категория пациентов: взрослые.
Пользователи протокола: врачи-онкологи, химиотерапевты, хирурги, врачи общей практики, врачи скорой неотложной медицинской помощи.
Шкала уровня доказательности:
| А | Высококачественный мета-анализ, систематический обзор РКИ или крупное РКИ с очень низкой вероятностью (++) систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию |
| В | Высококачественный (++) систематический обзор когортных или исследований случай-контроль или высококачественное (++) когортное или исследований случай-контроль с очень низким риском систематической ошибки или РКИ с невысоким (+) риском систематической ошибки, результаты которых могут быть распространены на соответствующую популяцию |
| С | Когортное или исследование случай-контроль или контролируемое исследование без рандомизации с невысоким риском систематической ошибки (+), результаты которых могут быть распространены на соответствующую популяцию или РКИ с очень низким или невысоким риском систематической ошибки (++ или +), результаты которых не могут быть непосредственно распространены на соответствующую популяцию |
| D | Описание серии случаев или неконтролируемое исследование или мнение экспертов |
| GPP | Наилучшая клиническая практика |
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
| Т1 | опухоли размерами менее 5 см |
| Т2 | более 5 см |
| N0 | отсутствие метастатического поражения лимфатических узлов |
| N1 | наличие метастатического поражения лимфатических узлов |
| G1 | высокодифференцированные |
| G2 | умеренно дифференцированные |
| G3 | низкодифференцированные |
| G4 | недифференцированные |
| Стадия la | G1-2T1N0M0 |
| Стадия lb | G1-2T2N0M0 |
| Стадия II | G3-4T1N0M0 |
| Стадия III | G3-4T2N0M0 |
| Стадия IV | любая G, любая T1-2N0-1М0-1 |
NB! Недостатком классификации AJCC (1997г) является то, что локализация опухоли в забрюшинном пространстве не учитывается при стадировании опухоли. Кроме того, первичные опухоли, обозначаемые символом Т2, объединяют опухоли с различным прогнозом.
Неблагоприятными факторами прогноза являются размеры опухоли более 5 см, низкая степень дифференцировки, микроскопически нерадикальное оперативное вмешательство.
М – отдаленные метастазы
| Мх | недостаточно данных для определения отдаленных метастазов |
| М0 | нет отдаленных метастазов |
| М1 | есть отдаленные метастазы |
рTNM патоморфологическая классификация
Категории pT, pN и рМ отвечают категориям Т, N и М.
Гистологическая классификация внеорганных забрюшинных опухолей.
Наибольшее распространение получила классификация Ассегmann (1954), который называет разделение опухолей данной локализации условным и в основу его кладет гистогенетический принцип:
I. Опухоли мезодермального происхождения
Опухоли из жировой ткани:
• злокачественные липосаркомы.
• злокачественные лейомиосаркома
• злокачественные фибросаркома
• злокачественные рабдомиосаркома.
• гемангиоперицитома – доброкачественная и злокачественная
• злокачественная лимфангиосаркома
• злокачественные миксосаркома
| Опухоли из закладок нервных влагалищ | • нейрофиброма, без капсулы; • инкапсулированная нейролеммома; • злокачественная нейролеммома (злокачественная шваннома). |
| Опухоли из тканей симпатической нервной системы | • ганглионеврома; • симпатобластома; • нейробластома. |
| Опухоли из гетеротопных тканей коры надпочечников и хромаффинных тканей | • рак из клеток надпочечника; • злокачественная нейромаффинная парагангиома; • парагангиома; • активная феохромоцитома. |
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ
Диагностические критерии
Жалобы и анамнез
· наличие пальпируемого опухолевого образования в животе;
· боли в животе – от тупых, ноющих незначительных болей до сильных, приступообразных;
· желудочный дискомфорт – потеря аппетита, отрыжка, иногда рвота, чувство тяжести в верхней половине живота;
· кишечные расстройства – запоры, поносы, чередование запоров с поносами, урчание и вздутие живота;
· нарушение общего состояния больного – общее недомогание, повышенная утомляемость, слабость, похудание, лихорадка, бледность кожных покровов;
· наличие пальпируемой опухоли.
NB! типичным признаком забрюшинных опухолей является отсутствие специфических симптомов. Клиническая картина заболевания обусловлена не видом новообразования, а его локализацией, близостью тех или иных органов и анатомических образований (кровеносных сосудов, нервов, лимфатических протоков) и их прорастанием.
Физикальное обследование:
Данные объективного исследования:
· осмотр: бледность кожных покровов, ассиметрия живота;
· пальпация живота: пальпаторное обнаружение опухоли, зависит от стадии заболевания, анатомической формы роста, напряжения брюшной стенки;
· перкуссия живота: притупление над опухолью.
Лабораторные исследования:
· общий анализ крови – характерны гипохромная анемия, повышение СОЭ, лейкоцитоз;
· анализ кала на скрытую кровь – положительная реакция при прорастании опухолью толстой кишки;
· коагулограмма – наблюдаются признаки гиперкоагуляции;
· анализ крови на онкомаркеры: АФП, РЭА – повышаются (не всегда).
Инструментальные исследования:
· УЗИ органов брюшной полости и забрюшинного пространства – с целью уточнения распространенности опухолевого процесса, прорастания опухоли в соседние органы и структуры, выявления отдаленных метастазов в печени и забрюшинных лимфоузлах;
· КТ/МРТ – с целью уточнения распространенности опухолевого процесса, прорастания опухоли в соседние органы и структуры, выявления отдаленных метастазов в печени и забрюшинных лимфоузлах;
· рентгеногафия грудной клетки в двух проекциях, при необходимости рентгеновская томография, компьютерная томография – для выявления метастазов в легких (по показаниям);
· ПЭТ – один из наиболее чувствительных и информативных методов выявления «маленьких» опухолей, рецидивов, микрометастазов.
Показания для консультации узких специалистов
· консультация других узких специалистов – по показаниям.
Диагностический алгоритм:
Дифференциальный диагноз
Дифференциальный диагноз и обоснование дополнительных исследований:
Внеорганные забрюшинные опухоли дифференцируют опухолями, с кистами почек и яичников. Применяемые в настоящее время специальные методы исследования дают возможность у большинства больных правильно поставить диагноз.
Необходимо помнить и о новообразованиях мочеточников, хотя они встречаются крайне редко. Ошибки в дифференциальной диагностике забрюшинных новообразований и опухолей желудочно-кишечного тракта встречаются реже и, как правило, обусловлены недостаточным обследованием больного или неправильной трактовкой рентгенологических данных.
К числу заболеваний, которые могут симулировать внеорганные забрюшинные опухоли, относится также аневризма брюшной аорты и ее ветвей.
Забрюшинные лимфатические узлы являются зоной как регионарных, так и отдаленных метастазов из опухолей различных органов. Возможность вторичных новообразований в этой области следует учитывать при дифференциальной диагностике забрюшинных опухолей. Кроме перечисленных выше опухолей, забрюшинно могут локализоваться неспецифические и специфические воспалительные процессы, паразитарные кисты, гематомы.
Лечение
Препараты (действующие вещества), применяющиеся при лечении
| Амикацин (Amikacin) |
| Аминокапроновая кислота (Aminocaproic acid) |
| Аминофиллин (Aminophylline) |
| Ацетилсалициловая кислота (Acetylsalicylic acid) |
| Винкристин (Vincristine) |
| Гемцитабин (Gemcitabine) |
| Гепарин (Heparin) |
| Гидроксиэтилкрахмал (Hydroxyethyl starch) |
| Дакарбазин (Dacarbazine) |
| Дактиномицин (Dactinomycin) |
| Дарбэпоэтин альфа (Darbepoetin alfa) |
| Дексаметазон (Dexamethasone) |
| Декстран (Dextran) |
| Декстроза (Dextrose) |
| Диклофенак натрия (Diclofenac sodium) |
| Дифенгидрамин (Diphenhydramine) |
| Доксорубицин (Doxorubicin) |
| Дротаверин (Drotaverinum) |
| Железа (III) гидроксид декстран (Ferric (III) hydroxide destrane) |
| Железа (III) гидроксид полимальтозат (Ferric (III) hydroxide polymaltosate) |
| Иматиниб (Imatinib) |
| Имипенем (Imipenem) |
| Инсулин человеческий (Insulin human) |
| Ифосфамид (Ifosfamide) |
| Кетопрофен (Ketoprofen) |
| Комплекс аминокислот для парентерального питания (Complex of amino acids for parenteral nutrition) |
| Месна (Mesna) |
| Метоклопрамид (Metoclopramide) |
| Метронидазол (Metronidazole) |
| Надропарин кальция (Nadroparin calcium) |
| Натрия хлорид (Sodium chloride) |
| Неостигмина метилсульфат (Neostigmine methylsulfate) |
| Ондансетрон (Ondansetron) |
| Офлоксацин (Ofloxacin) |
| Пазопаниб (Pazopanib) |
| Парацетамол (Paracetamol) |
| Платифиллин (Platifillin) |
| Преднизолон (Prednisolone) |
| Спиронолактон (Spironolactone) |
| Теофиллин (Theophylline) |
| Тофизопам (Tofisopam) |
| Трабектедин (Trabectedin) |
| Трамадол (Tramadol) |
| Филграстим (Filgrastim) |
| Флуконазол (Fluconazole) |
| Фуросемид (Furosemide) |
| Хлоропирамин (Chloropyramine) |
| Цефазолин (Cefazolin) |
| Цефепим (Cefepime) |
| Цефтазидим (Ceftazidime) |
| Цефтриаксон (Ceftriaxone) |
| Цефуроксим (Cefuroxime) |
| Циклофосфамид (Cyclophosphamide) |
| Циластатин (Cilastatin) |
| Ципрофлоксацин (Ciprofloxacin) |
| Эноксапарин натрия (Enoxaparin sodium) |
| Эпоэтин альфа (Epoetin alfa) |
| Этамзилат (Etamsylate) |
| Этопозид (Etoposide) |
Лечение (амбулатория)
ТАКТИКА ЛЕЧЕНИЯ НА АМБУЛАТОРНОМ УРОВНЕ
Медикаментозное лечение, хирургическое вмешательство: нет.
Дальнейшее ведение:
Профилактические мероприятия:
Факторы риска:
· питание – пища с преобладанием животных жиров, белков и рафинированных углеводов (сахар);
· малоподвижный образ жизни (гипокинезия, ожирение, возраст старше 50 лет);
· курение, злоупотребление алкоголем;
· нестероидные противовоспалительные препараты;
· отягощенный семейный анамнез;
· злокачественная опухоль в анамнезе;
Первичная профилактика: здоровый образ жизни, регулирование режима питания, формирование «групп риска».
Индикаторы эффективности лечения: смотреть Стационарный уровень.
Лечение (стационар)
ТАКТИКА ЛЕЧЕНИЯ НА СТАЦИОНАРНОМ УРОВНЕ
Тактика лечения:
· ликвидация опухолевого очага и метастазов;
· достижение полной или частичной регрессии, стабилизации опухолевого процесса.
Тактика лечения:
· Стадия Ia (Т1b N0, NX M0, низкая степень злокачественности): хирургическое удаление опухоли.
· Стадия Ib (Т2b N0, NX M0, низкая степень злокачественности): хирургическое удаление опухоли + послеоперационная лучевая терапия на область резидуальной опухоли в СОД 60–70 Гр, РОД 2 Гр (при R1, R2).
· Стадии II–III (Т1b–Т2b N0, N1 M0, высокая степень злокачественности): хирургическое удаление опухоли (при N+ выполняется лимфодиссекция) + послеоперационная лучевая терапия (СОД 40–50 Гр, РОД 2 Гр) + 3–4 курса адъюванной химиотерапии (при чувствительных гистологических типах опухоли).
При R1, R2 суммарная очаговая доза лучевой терапии на область ре-
зидуальной опухоли должна быть увеличена до 60–70 Гр (без превышения толерантных доз на здоровые органы и ткани).
При сомнении в резектабельности или нерезектабельной опухоли проводится курс лучевой терапии в СОД 40–50 Гр в режиме классического фракционирования и/или 2–3 курса химиотерапии (предпочтительнее в условиях общей или регионарной гипертермии).
При сохранении нерезектабельности опухоли проводится лучевая терапия
до СОД 60–70 Гр за весь курс лечения ± 3–4 курса химиотерапии (схема лечения
определяется исходя из оценки эффективности неоадъювантной химиотерапии по данным компьютерной томографии или ультразвукового исследования).
· Стадия IV (любая Т и N M1, любая степень злокачественности):
паллиативное лечение по индивидуальным программам с включением химиотерапии и/или лучевой терапии, в том числе в модифицированных условиях (общая и регионарная гипертермия);
хирургические вмешательства для уменьшения опухолевой массы и ликвидации симптомов опухолевой компрессии. Резекция отдаленных метастазов оправдана при контролируемом опухолевом процессе.
NB! при резектабельной опухоли и наличии одиночных и единичных метастазов в отдаленных органах – циторедуктивная операция с одномоментным или отсроченным удалением метастазов.
Критерии резектабельности метастазов в печени – отсутствие нерезектабельных экстрапеченочных метастазов, функциональная переносимость и отсутствие сопутствующих заболеваний в стадии суб – и декомпенсации), возможность удаления всех метастазов с клиренсом не менее 0,1 см без опухолевого роста и поражение менее 70% или 6 сегментов печени.
Критерии эффективности лечения:
· полный эффект – исчезновение всех очагов поражения на срок не менее 4-х недель;
· частичный эффект – большее или равное 50% уменьшение всех или отдельных опухолей при отсутствии прогрессирования других очагов;
· стабилизация – (без изменений) уменьшение менее чем на 50% или увеличение менее чем на 25% при отсутствии новых очагов поражения;
· прогрессирование – увеличение размеров одной или более опухолей более 25% либо появление новых очагов поражения
Немедикаментозное лечение
· Режим – больного при проведении консервативного лечения – общий. В ранний послеоперационный период – постельный или полупостельный (в зависимости от объема операции и сопутствующей патологии). В послеоперационном периоде – палатный.
· Диета – Стол №1 после хирургического лечения, затем переход на Стол №2.
· Лучевая терапия:
Послеоперационная лучевая терапия показана при степени местного распространения соответствующей St Ib – St IV.
Проводится послеоперационная лучевая терапия на область резидуальной опухоли в СОД 60–70 Гр, РОД 2 Гр (при R1, R2).
При сомнении в резектабельности или нерезектабельной опухоли проводится курс лучевой терапии в СОД 40–50 Гр в режиме классического фракционирования.
Лучевая терапия проводится в конвенциальном (стандартном) или конформном режиме облучения в статическом многопольном режиме РОД 2-2,5-3,0 Гр до СОД 40–60Гр на зону врастания опухоли. При проведении лучевой терапии возможно применение препаратов, защищающих организм от лучевого повреждения.
Облучение проводят на гамма-терапевтических аппаратах или линейных ускорителях.
Медикаментозное лечение
Химиотерапия нейроэндокринных опухолей:
Химиотерапия назначается при невозможности хирургического лечения, после циторедуктивных операций.
Функционирующие НЭО G1-G3: аналоги соматостатина (симптоматическая терапия):
Октреотид 0,1 мг п/к, 3 раза в сутки в течение короткого периода времени (примерно 2 недели) с целью оценки его эффективности и общей переносимости
затем
Октреотид ЛАР 20 мг внутримышечно 1 раз в 28 дней.
Если в течение 3 месяцев обеспечивается адекватный контроль клинических проявлений и биологических маркеров заболевания – октреотид ЛАР 10 мг, внутримышечно 1 раз/28 дней.
Если в течение 3 месяцев обеспечивается только частичный контроль клинических проявлений и биологических маркеров заболевания – октреотид ЛАР 30 мг внутримышечно каждые 4 недели.
Распространенные нейроэндокринные опухоли толстой кишки или с неизвестной локализацией первичной опухоли – октреотид ЛАР 30 мг внутримышечно 1раз/28 дней до прогрессирования.
Нефункционирующие НЭО:
Ki67 20%, G3:
· карбоплатин/цисплатин+этопозид;
· темозоломид+бевацизумаб;
· аналоги соматостатина.
Практические рекомендации по лекарственному лечению гастроинтестинальных стромальных опухолей (GIST)
Лечение нерезектабельных опухолей при рецидиве или метастатической болезни
Терапия первой линии:
При нерезектабельных опухолях, рецидиве или метастатической болезни основной метод лечения – таргетная терапия иматинибом 400 мг в сутки. При выявлении мутации в 9-м экзоне гена KIT рекомендован иматиниб 800 мг в сутки (достоверно увеличивает время до прогрессирования без статистически значимого улучшения общей выживаемости). При прогрессировании на фоне приема иматиниба в дозе 400 мг в сутки показана эскалация дозы до 800 мг в сутки. При исходно нерезектабельных опухолях у больных с эффектом в результате терапии целесообразна оценка возможности радикального хирургического лечения через 6–12 месяцев после начала терапии.
Терапия второй линии:
При прогрессировании заболевания на фоне приема иматиниба (после эскалации дозы с 400 до 800 мг), непереносимости иматиниба либо первичной резистентности показана терапия сунитинибом: 50 мг в сутки, 4 недели с двухнедельным перерывом. При выраженных побочных эффектах допустимо снижение дозы до 37,5 мг в сутки.
Саркомы мягких тканей
Распространенный опухолевый процесс – стадия III–IV:
Химиотерапия является основным методом лечения диссеминированного процесса при мягкотканых саркомах. Наиболее часто используются доксорубицин, ифосфамид, дакарбазин. Стандартом химиотерапии диссеминированных сарком мягких тканей первой линии является комбинированный режим доксорубицин + ифосфамид. Для пациентов старше 65 лет методом выбора является монотерапия антрациклинами. При общем хорошем состоянии комбинированная химиотерапия предпочтительнее, когда ожидается выраженный эффект со стороны опухоли. При поверхностных ангиосаркомах альтернативой является назначение таксанов, показавших высокую противоопухолевую активность при данном гистологическом типе. Паклитаксел показал высокую эффективность в терапии местнораспространенных ангиосарком, в частности ассоциированных с синдромом Стюарта-Тривса.
В качестве >2 линии в лечении липосарком, лейомиосарком, синовиальной и экстраоссальной формы саркомы Юинга может быть использован трабектедин. Также во вторую и более линии для большинства гистологических подтипов, за исключением липосарком и GIST, может быть использован пазопаниб. Для липосарком возможно использование эрибулина. Гемцитабин показал наличие противоопухолевой активности в качестве единственного противоопухолевого агента и при лейомиосаркоме. Дакарбазин, назначенный в качестве второй линии химиотерапии, также обладает некоторой противоопухолевой активностью (вероятно, более всего в лечении лейомиосаркомы. Пазопаниб используется в качестве второй и более линий для лечения большинства гистологических подтипов, однако для химиорезистентных гистотипов (альвеолярная саркома мягких тканей, светлоклеточная саркома мягких тканей, солитарная фиброзная опухоль/гемангиоэндотелиома) должен применяться в первую линию лечения.
Наблюдение у больных, закончившим этап комбинированного лечения, динамическое наблюдение проводится каждые 3 месяца в течение первых 2 лет, далее раз в 6 месяцев до 5 лет.
Перечень основных лекарственных средств:
| Химиопрепараты | УД | ||
| № | МНН препарата | Доза, кратность, способ применения и длительность применения | |
| 1 | Доксорубицин | Дозировка и кратность согласно режимам химиотерапии, в/в | В |
| 2 | Ифосфамид | Дозировка и кратность согласно режимам химиотерапии, в/в | В |
| 3 | Гемцитабин | Дозировка и кратность согласно режимам химиотерапии, в/в | В |
| 4 | Трабектидин | Дозировка и кратность согласно режимам химиотерапии, в/в | В |
| 5 | Пазопаниб | Дозировка и кратность согласно режимам химиотерапии, в/в | В |
| 6 | Месна | Дозировка и кратность согласно режимам химиотерапии, в/в | В |
| 7 | Дакарбазин | Дозировка и кратность согласно режимам химиотерапии, в/в | В |
| 8 | Дактиномицин | Дозировка и кратность согласно режимам химиотерапии, в/в | В |
| 9 | Циклофосфамид | Дозировка и кратность согласно режимам химиотерапии, в/в | В |
| 10 | Этопозид | Дозировка и кратность согласно режимам химиотерапии, в/в | В |
| 11 | Иматиниб | Дозировка и кратность согласно режимам химиотерапии, в/в | В |
| 12 | Винкристин | Дозировка и кратность согласно режимам химиотерапии, в/в | В |
| 13 | Эпоэтин альфа | 40 тысяч МЕ, 3 раза в неделю, по показаниям в течение 1 месяца, подкожно, внутривенно | А |
| 14 | Дарбопоэтин альфа | 2,25мкг/м 2 1 раз в 7 дней в течение 9 недель, подкожно | А |
| 15 | Филграстим | 30 млн ЕД, ежедневно по показаниям, подкожно | А |
Хирургическое вмешательство:
Основным методом лечения внеорганных забрюшинных опухолей является хирургический.
Цель:
· радикальное удаление опухоли.
Название вмешательства:
· тотальное или субтотальное удаление опухоли.
Показания к вмешательству:
· наличие внеорганного забрюшинного образования.
Противопоказания к вмешательству:
· тяжелая сопутствующая патология в стадии декомпенсации.
Методика проведения:
· полное удаление образования в пределах анатомической области.
Дальнейшее ведение:
Наблюдение:
Режим наблюдения:
· первый год – 1 раз в 3 мес.;
· второй год – 1 раз в 6 мес.;
· в последующем, пожизненно – 1 раз в год.
Объем обследования (по показаниям):
· ОАК, БАК, ОАМ, коагулограмма;
· ультразвуковое исследование брюшной полости, забрюшинного пространства;
· рентгенография обзорная органов грудной клетки (1 проекция);
· МРТ, КТ органов брюшной полости и забрюшинного пространства;
· ПЭТ (по показаниям);
· другие методы исследования (экскреторная урография, ФЭГДС и т.д.) и консультации специалистов (гинеколог, уролог и др.) по показаниям.
Индикаторы эффективности лечения:
· удовлетворительное состояние при условии отсутствия осложнений и заживления послеоперационной раны;
· данные, свидетельствующие об отсутствии признаков прогрессирования процесса, полученные клиническими и/или визуализирующими методами исследования, а также повышение качества жизни больного.
Госпитализация
ПОКАЗАНИЯ ДЛЯ ГОСПИТАЛИЗАЦИИ С УКАЗАНИЕМ ТИПА ГОСПИТАЛИЗАЦИИ
Показания для плановой госпитализации:
· подозрение или верифицированное внеорганное забрюшинное образование, II клиническая группа
Показания для экстренной госпитализации:
· острая кишечная непроходимость;
· внутреннее кровотечение;
· распад опухоли;
· болевой синдром.
Информация
Источники и литература
Информация
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ПРОТОКОЛА
Список разработчиков протокола:
1) Кузикеев Марат Анатольевич – доктор медицинских наук, РГП на ПХВ «Казахский научно – исследовательский институт онкологии и радиологии», руководитель центра абдоминальной онкологии.
2) Джуманов Абай Игликович – врач Центра абдоминальной онкологии, РГП на ПХВ «Казахский научно-исследовательский институт онкологии и радиологии»
3) Трущенко Олег Юрьевич лучевой терапевт Центра абдоминальной онкологии, РГП на ПХВ «Казахский научно-исследовательский институт онкологии и радиологии».
4) Омарова Индира Милатовна, заведующая отделением химиотерапии РГП на ПХВ «Областной онкологический диспансер Карагандинской области».
5) Курманалиев Аль-Фараби Канатович – химиотерапевт «Центра опухолей костей мягких тканей и меланом» РГП на ПХВ «Казахский научно-исследовательский институт онкологии и радиологии».
6) Чингисова Жанна Казбековна – заместитель директора по клинике РГП на ПХВ «Казахский научно-исследовательский институт онкологии и радиологии».
7) Аманов Тайман Тулегалиевич – кандидат медицинских наук, заместитель директора по лечебной работе ГКП на ПХВ «Областной онкологической диспансер ЗКО»
8) Табаров Адлет Берикболович – клинический фармаколог, начальник отдела инновационного менеджмента РГП на ПХВ «Больница медицинского центра Управление делами Президента РК».
Указание на отсутствие конфликта интересов: нет.
Рецензенты:
1) Джураев Миржалол Дехканович – доктор медицинских наук, профессор, заведующий онкоабдоминальным отделением, Республиканский Научный Центр Онкологии Республики Узбекистан.
Указание условий пересмотра протокола: Пересмотр протокола через 5 лет после его опубликования и с даты его вступления в действие или при наличии новых методов с уровнем доказательности.