что такое полиморфизмы в генах
Что такое полиморфизмы в генах
Большинство оценок частоты мутаций использует обнаружение патологических мутаций с явным влиянием на фенотип. Тем не менее существует масса непатогенных мутаций, считающихся относительно нейтральными; а некоторые могут даже быть полезными. В ходе эволюции устойчивый приток новых изменений нуклеотидов гарантировал высокую степень генетического разнообразия и индивидуальности.
Это распространяется на все области генетики человека и медицинской генетики. Генетическое разнообразие может проявляться в виде изменений в окраске хромосом, изменения числа копий сегментов ДНК, нуклеотидных замен в ДНК, изменений в белках или же как болезнь.
ДНК последовательности каждого участка хромосомы в высшей степени сходны у большинства людей в мире. Фактически произвольно выбранный сегмент ДНК человека размером около 1000 пар оснований содержит, в среднем, только одну пару, отличающуюся на двух гомологичных хромосомах, унаследованных от родителей (если предположить, что родители не родственники).
Эта почти в 2,5 раза больше, чем оценка доли гетерозиготных нуклеотидов для кодирующих белок областей генома (примерно 1 на 2500 пар оснований). Различие неудивительное, поскольку интуитивно понятно, что регионы, кодирующие белок, находятся под более жестким давлением отбора, и таким образом встречаемость мутаций в таких регионах в эволюции должна быть более низкой.
Когда вариант встречается настолько часто, что его обнаруживают более чем в 1% хромосом в общей популяции, его называют генетическим полиморфизмом. Аллели с частотами менее чем 1% принято называть редкими вариантами. Хотя много патологических мутаций, приводящих к генетическим болезням — редкие варианты, нет простой корреляции между частотой аллеля и его влиянием на здоровье. Много редких вариантов не имеют патогенных эффектов, тогда как некоторые варианты, достаточно частые, чтобы считаться полиморфизмами, предрасполагают к тяжелым болезням.
Существует много типов полиморфизма. Некоторые полиморфизмы — следствие вариантов, вызванных делециями, дупликациями, утроениями и так далее, сотен миллионов пар оснований ДНК, и не связаны с каким-либо известным патологическим фенотипом; другие изменения аналогичного размера оказываются редкими вариантами, явно вызывающими тяжелые болезни. Полиморфизмами могут оказаться изменения в одном или нескольких основаниях ДНК, расположенных между генами или в интронах, не связанные с функционированием генов и обнаруживаемые только прямым анализом ДНК.
Изменения последовательности нуклеотидов могут располагаться в кодирующей последовательности самого гена и приводить к образованию различных вариантов белков, в свою очередь вызывающих четко очерченные фенотипы. Изменения в регуляторных областях также могут быть важными в определении фенотипа, влияя на транскрипцию или стабильность мРНК.
Полиморфизм — ключевой элемент в исследовании и практическом использовании генетики человека. Способность различать унаследованные формы генов или других сегментов генома обеспечивают инструментальные средства, необходимые для широкого спектра приложений. Как показано в этой и последующих главах, генетические маркеры — мощное научно-исследовательское инструментальное средство картирования генов на конкретном регионе хромосомы при анализе сцепления или аллельной ассоциации.
Они уже широко используются в медицине — от пренатальной диагностики наследственных болезней до обнаружения гетерозиготного носительства, а также в банках крови и тканей для типиро-вания перед переливаниями и пересадками органов (см. далее в этой главе).
Полиморфизм — основа для развивающихся мероприятий по обеспечению основанной на геномике персонализированной медицины, когда медицинские мероприятия индивидуально подбирают на основе анализа полиморфных вариантов, увеличивающих или уменьшающих риск частых болезней взрослого возраста (например, заболевания коронарных сосудов сердца, опухолей и сахарного диабета), возникновения осложнений после хирургических вмешательств или влияющих на эффективность и безопасность конкретного лекарственного препарата. Наконец, анализ полиморфизма стал мощным новым средством в судебных приложениях, например, определении отцовства, определении останков жертв преступления или для сопоставления ДНК подозреваемого и преступника.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Генетический полиморфизм, ассоциированный с риском развития тромбофилии
Тромбофилия (от греч. trhombos – сгусток и philia – склонность) – состояние системы крови, которое проявляется в нарушении гемостаза, склонности к развитию рецидивирующих сосудистых тромбозов (преимущественно венозных) различной локализации и часто возникает в
связи с беременностью, после хирургического вмешательства, травмы или физического пере-
напряжения. Заболевание обусловлено генетической (у 30–50 % с тромботическим состоянием) или приобретенной патологией клеток крови, а также дефектами свертывающей системы крови. При этом тромбофилия еще не тромбоз, но при этом наблюдается готовность организма к тромбообразованию.
Генетическая предрасположенность к тромбофилии может реализоваться через генетические дефекты как свертывающей, так и противосвертывающей (антикоагулянтной и фибринолитической) систем крови, при которых имеется готовность к тромбозу. Тромбозом называют прижизненное образование сгустков крови в просвете сосудов или в полостях сердца.
Тромбозы играют одну из главных ролей в развитии заболеваний сердечно-сосудистой системы, которые стоят на первом месте в инвалидизации и преждевременной смертности жителей экономически развитых стран. На сегодняшний день доля этих заболеваний в структуре смертности составляет 40–60 % (примерно 14 миллионов смертей ежегодно). При этом продолжающийся рост заболеваемости и поражение людей все более молодого возраста делает сердечно-сосудистые заболевания (ССЗ) важнейшей медико-социальной проблемой здравоохранения. Показатели смертности от ССЗ в России в 2–4 раза выше, чем в западноевропейских странах, США, Канаде, Австралии, и в настоящее время наблюдается тенденция к росту смертности. Согласно статистике последних лет, опубликованной на сайте http://www.critical.ru, в структуре смертности от ССЗ в российской популяции 85,5 % приходится на долю ИБС (46,8 %) и мозгового инсульта (38,7 %). Наследственная тромбофилия играет важную роль в структуре акушерских и гинекологических осложнений, таких как потери плода, привычное невынашивание беременности, повторные неудачи при ЭКО, тромбоэмболии у беременных.
Еще одной важной проблемой является назначение оральных контрацептивов. Оральная контрацепция является одним из самых надежных способов предотвращения нежелательной беременности, но сопряжена с риском тромбозов. Показано, что сама по себе гормональная контрацепция незначительно повышает риск тромбозов, но при носительстве определенного генотипа опасность резко возрастает. Согласно Национальным медицинским критериям приемлемости методов контрацепции 2012 года и четвертой редакции «Медицинских критериев приемлемости для использования методов контрацепции», разработанных ВОЗ в 2009 году, для предотвращения тромбозов и тромбоэмболических осложнений при приеме оральных контрацептивов рекомендовано выявление тромбогенных мутаций (F2 – протромбиновая мутация, F5 – фактор Лейдена).
Генетический анализ позволяет выявить полиморфизмы генов факторов системы гемостаза, обусловливающих их аномальный синтез или нарушение функциональной активности. Это помогает оценить риски развития сердечно-сосудистой патологии и акушерско-гинекологических осложнений, тромбоэмболии, венозных и артериальных тромбозов. Скрининг генетических особенностей тромбофилий помогает на раннем этапе выявить группу риска и внести соответствующие коррективы в тактику ведения пациентов.
Показания к назначению профиля «генетика тромбофилии»:
единичный до 50 лет;
в любом возрасте при наличии семейного анамнеза;
необычной локализации (портальные, брыжеечные, мозговые вены);
непонятной этиологии после 50 лет;
массивные хирургические вмешательства;
Полиморфизм гена коагуляционного фактора II(G20210A) (протромбин)
Настоящая мутация наследуется по аутосомно-доминантному типу и в гетерозиготном состоянии встречается у 2,3 % людей в общей популяции. Клинически ее можно заподозрить по постоянно высокому уровню протромбина в плазме крови (у 87% носителей превышает 115%). Риск развития тромбоза у носителей гетерозиготной аномалии повышается в 3 – 5 раз и более значительно при использовании оральных контрацептивов.
Показания к назначению: инфаркт миокарда, гиперпротромбинемия, тромбоэмболические состояния в анамнезе, невынашивание беременности, фетоплацентарная недостаточность, внутриутробная гибель плода и задержка развития плода, отслойка плаценты, перед большими полостными операциями.
Биологический материал для анализа : цельная кровь, стабилизированная ЭДТА
Полиморфизм гена коагуляционного фактора V (акцелератор-глобулин) (Лейден)
Мутация наследуется по аутосомно-доминантному типу. Аллельная частота от 2,9 до 7,8% (в среднем 4,4%). FVL (Лейден) увеличивает риск преимущественно венозного тромбоза у лиц моложе 40 – 45 лет в 3 – 4 раза, особенно на фоне беременности, послеродового периода, длительной иммобилизации, больших хирургических вмешательств и приема оральных контрацептивов.
Показания к назначению: венозный тромбоз, тромбоэмболические заболевания в молодом возрасте, рецидивирующие тромбоэмболии, сердечно-сосудистые заболевания в семейном анамнезе, невынашивание беременности, фетоплацентарная недостаточность, внутриутробная гибель плода и задержка развития плода, отслойка плаценты, перед большими полостными операциями, прием пероральных контрацептивов.
Биологический материал для анализа : цельная кровь, стабилизированная ЭДТА
Полиморфизм гена коагуляционного фактора VII(G10976A) (проконвертин)
Вариант 353Gln (10976A) приводит к понижению производительности (экспрессии) гена фактора VII и является защитным фактором в развитии тромбозов и инфаркта миокарда. Распространенность данного варианта в европейских популяциях составляет 10-20%. При исследовании пациентов со стенозом коронарных артерий и инфарктом миокарда обнаружено, что наличие мутации 10976A приводит к понижению уровня фактора VII в крови на 30% и 2-х кратному понижению риска инфаркта миокарда даже при наличии заметного коронарного атеросклероза.
Показания к назначению: оценка риска инфаркта миокарда и фатального исхода при инфаркте миокарда, тромбоэмболические заболевания в анамнезе.
Биологический материал для анализа : цельная кровь, стабилизированная ЭДТА
Полиморфизм гена коагуляционного фактора XIII(G103T) (фибриназа)
Биологический материал для анализа : цельная кровь, стабилизированная ЭДТА
Полиморфизм гена коагуляционного фактора I(G455A) (фибриноген)
Показания к назначению: повышенный уровень фибриногена плазмы, повышенное кровяное давление, повышенная вероятность тромбообразования, инсульт.
Биологический материал для анализа : цельная кровь, стабилизированная ЭДТА
Полиморфизм гена ингибитора активатора плазминогена PAI-1(5G/675/4G)
Показания к назначению: портальный тромбоз и другие тромбоэмболические состояния в анамнезе, инфаркт миокарда, ИБС, повышение концентрации ингибитора активатора плазминогена в крови, мутация ITGB3, ожирение.
Биологический материал для анализа : цельная кровь, стабилизированная ЭДТА
Полиморфизм гена тромбоцитарного рецептора (интегрина) ITGA2(C807T)
Данный рецептор, влияет на адгезию тромбоцитов на коллагене и других субстратах, а также участвует в реорганизации межклеточного матрикса. Генетические варианты GPIa могут приводить к изменению кинетики адгезии тромбоцитов. Вариант C807T встречается с частотой 5,7% и является маркером кардиоваскулярных заболеваний и артериальным тромбоэмболиям. Исследование 177 пациентов с инфарктом миокарда (средний возраст 57 лет) и 89 здоровых доноров показало значительную разницу в распределении частот вариантов 807C и 807T между двумя группами. Более высокая частота гомозиготного варианта 807T у пациентов соответствовала почти 3-кратному повышению риска инфаркта
Показания к назначению: cемейный анамнез ранней ИБС, инфаркт миокарда, тромбоэмболические состояния в анамнезе, постангиопластические тромбозы, неонатальная тромбоцитопения, антитромботическая терапия аспирином.
Биологический материал для анализа : цельная кровь, стабилизированная ЭДТА
Полиморфизм гена тромбоцитарного рецептора (интегрина) ITGB3(T1565C)
Ген тромбоцитарного рецептора фибриногена (ITGB3) кодирует бета-3 субъединицу интегрин-комплекса поверхностного рецептора тромбоцитов GPIIb/IIIa, известную также как гликопротеин-3а (GPIIIa). ITGB3 участвует в межклеточной адгезии и сигнализации. ITGB3 обеспечивает взаимодействие тромбоцита с фибриногеном плазмы крови, что приводит к быстрой агрегации (склеиванию) тромбоцитов. Мутация 33P GPIIIa способствует повышенной склонности тромбоцитов к агрегации, что увеличивает риск развития сердечно-сосудистых заболеваний. У пациентов с этим вариантом часто отмечается пониженная эффективность аспирина как дезагрегантного препарата. Частота встречаемости мутации 33P в европейских популяциях составляет 8-15%.
Показания к назначению: Семейный анамнез ранней ИБС, инфаркт миокарда, тромбоэмболические состояния в анамнезе, постангиопластические тромбозы, неонатальная тромбоцитопения, антитромбозная терапия аспирином.
Биологический материал для анализа : цельная кровь, стабилизированная ЭДТА
Полиморфизмы генов, кодирующих ферменты метаболизма половых гормонов
Исследование полиморфизмов генов является генетическим исследованием. Поиск вариантов генов или полиморфизмов позволяет выявить варианты генов, которые оказывают неблагоприятное воздействие на организм. Например, полиморфизмы генов, отвечающих за свертывание крови важны при планировании беременности, поскольку наличие неблагоприятных аллелей (вариантов генов) может привезти к чрезмерному образованию тромбов и, как следствие, прерыванию беременности. Определение вариантов генов BRCA1 и BRCA2, CHEK2 помогает выявить риск развития рака молочной железы и начать превентивно менять свои привычки. Аналогичным образом, исследование полиморфизмов генов, кодирующих половые гормоны помогает исключить генетический фактор патологии репродуктивной сферы.
Половые гормоны
Половые гормоны относятся к группе стероидных гормонов. Стероидные гормоны помимо регулирования репродуктивной функции (прогестины, эстрогены, андрогены), отвечают за антистрессовые реакции (глюкокорткоиды) и солевой обмен (минералокортикоиды).
Общим предшественником синтеза всех стероидов является холестерин. Половые гормоны синтезируются, в основном, в яичках и яичниках, а также в коре надпочечников. Разнообразие путей биосинтеза в тканях обеспечивается действием различных ферментов, которые расположены в разных компартментах клетки — мембранах эндоплазматического ретикулума и в митохондриях.
Биосинтез и секреция половых гормонов в эндокринных железах контролируется гипофизарными гормонами: лютеинизирующим гормоном (ЛГ), фолликулостимулирующим гормоном (ФСГ). В свою очередь производство гормонов в гипофизе зависит от уровня, так называемых, высвобождающих факторов, которые образуются в верхней части мозга — гипоталамусе. Половые гормоны по механизму отрицательной обратной связи регулируют синтез гормонов гипофиза. Если концентрация половых гормонов высокая, то синтез тропных гормонов снижается, и, наоборот, при снижении концентрации половых гормонов, синтез и секреция гормонов-регуляторов возрастает.
 |
Мужские половые гормоны
Мужские половые гормоны вырабатываются в основном в мужских половых железах — в клетках Лейдига семенников (95%). Остальные 5% андрогенов образуются в коре надпочечников. Пути биосинтеза андрогенов в яичках и коре надпочечников одинаков.
Отщепление боковой цепи холестерола и образование прегненолона — первая реакция стероидогенеза. Однако, в отличие от аналогичной реакции, протекающей в надпочечниках, эта стадия стимулируется ЛГ, а не адренокортикотропным гормоном (АКТГ).
Тестостерон
Превращение прегненолона в тестостерон может протекать двумя путями: через образование прогестерона или дегидроэпиандростерона.
Суточная секреция тестостерона у мужчин составляет в норме примерно 5 мг и сохраняется на протяжении всей жизни организма. Гормон циркулирует в крови в связанной с белками плазмы форме: альбумином (40%) и специфическим глобулином, связывающим половым гормоном (ГСПГ). Лишь 2% от общего количества гормона в крови транспортируется в свободном виде и проявляют биологическую активность.
Дигидротестостерон
В семенных канальцах, предстательной железе, коже, наружных половых органах тестостерон служит предшественником более активного андрогена — дигидротестостерона. Это превращение происходит при участии фермента — 5α-редуктазы. В процессе участвует примерно 4% тестостерона. Семенники человека секретируют в сутки 50–100 мкг дигидротестостерона. Однако большое количество гормона — следствие периферических превращений. Суммарная суточная секреция дигидротестостерона составляет 400 мкг.
В некоторых периферических тканях, небольшое количество тестостерона превращается в эстрадиол. В качестве побочных продуктов клетки Лейдига также постоянно секретируют эстрадиол и прогестерон, хотя роль этих гормонов в развитии и поддержании функций размножения и формирования полового поведения у мужчин до конца не изучена.
Андрогены действуют на другие органы и ткани помимо гонад: эмбриональные вольфовы структуры, мышцы, кости, почки, мозг. Действие андрогенов различно в разные периоды жизни. У эмбриона под действием андрогенов органы репродукции формируются по мужскому типу. У плода мужского пола происходит маскулинизация мозга. Андрогены обладают мощным анаболическим действием и стимулируют клеточное деление, поэтому в пубертатном периоде происходит резкое увеличение линейных размеров тела, скелетных мышц, костей. Андрогены вызывают изменение структуры кожи и волос, снижение тембра голоса вследствие утолщения голосовых связок и увеличения объёма гортани, стимулируют секрецию сальных желёз.
Женские половые гормоны
В яичниках синтезируются женские половые гормоны — эстрогены и прогестины, среди которых наиболее активны 17β-эстрадиол и прогестерон.
Образование эстрогенов
Согласно современным представлениям, синтез женских половых гормонов идет через образование мужских половых гормонов. Образование эстрогенов яичников предполагает выработку андрогенов (андростендиона) в клетках теки фолликулов с последующей ароматизацией андрогенов в клетках гранулёмы. В клетках теки синтезируются рецепторы ЛГ. Рецепторы ФСГ образуются в клетках гранулёмы. ЛГ, связываясь с рецепторами клеток теки, активирует фермент, катализирующий превращение холестерола в прегненолон. Эта реакция стимулирует и образование основного андрогена яичников — андростендиона. ФСГ, взаимодействуя с рецепторами клеток гранулёмы, активирует содержащийся в этих клетках комплекс, который стимулирует превращение андрогенов в эстрогены.
Непосредственно в клетках теки синтезируется малое количество эстрогенов. Значительная часть эстрогенов продуцируется путём периферической ароматизации андрогенов в жёлтом теле, фетоплацентарном комплексе (во время беременности). Дополнительно эстрогены производятся в коре надпочечников, жировой ткани, печени, коже и других тканях, где присутствует повышенная ароматазная активность.
| Примерно 95% циркулирующих в крови эстрогенов связано с транспортными белками — ГСПГ и альбумином. Биологической активностью обладает только свободная форма эстрогенов. Эстрогены влияют на развитие вторичных женских половых признаков, вызывают размножение эндометрия и клеток молочной железы. Однако под влиянием эстрогенов находятся не только клетки репродуктивной сферы, но и кожа, мозг, кости, эндотелий сосудов, волосяные фолликулы. Различные нарушения в половой сфере достаточно легко предупредить, если знать о генетических особенностях ферментов, катализирующих наиболее важные реакции синтеза половых гормонов. К таким генам относятся 5а-редуктаза, SHBG, AR,CYP17. |  |
Ген: CYP17, 17a-гидроксилаза/17,20-лиаза
Полиморфизм: A1/A2 (5′- C/T)
Продукт гена — ключевой фермент биосинтеза стероидных гормонов в яичниках и надпочечниках. Фермент присоединяет гидрокси-группу (OH) к прегненолону и прогестерону в позиции 17-го атома углерода, в результате чего образуется 17-гидроксипрегненолон и 17-гидроксипрогестерон. Также в этих молекулах фермент рассекает связь между углеродами 17 и 20, в результате образуются дегидроэпиандростерон и андростендион соответсвенно.
Повышенный уровень андрогенов (мужских половых гормонов) может быть обусловлен полиморфизмом гена CYP17, генотипы A1/A2 и A2/A2 которого соответствуют предрасположенности к невынашиванию беременности.
Ген 5 альфа-редуктаза
Полиморфизм: Val89Leu (V89L)
Фермент α-редуктаза типа 2А катализирует превращение тестостерона в биологически активную форму дигидротестостерон. Ключевой фермент в эффектах андрогенов.
Ген: SHBG, глобулин, связывающий половые гормоны (ГСПГ)
Полиморфизм: STR TAAAA(n) (полиморфизм коротких повторяющихся последовательностей).
Перенос андрогенов из источника их продукции к месту назначения происходит в связанном виде с глобулином, связывающим половые гормоны, который синтезируется в печени. Степень биологической активности андрогенов определяется уровнем свободных андрогенов (связанные с ГСПГ стероиды биологически не активны). Одной из причин высокого уровня свободного тестостерона является снижение уровня ГСПГ, с которым связывается 65% циркулирующего в крови тестостерона. Вследствие снижения уровня ГСПГ возрастает скорость превращения андростендиона в тестостерон. Снижение уровня ГСПГ в сыворотке крови происходит при ожирении, циррозе печени, вирусных гепатитах, гипотиреозе, акромегалии и лечении кортикостероидами. Низкий уровень ГСПГ в сыворотке крови может быть обусловлен сочетанием генетических и негенетических факторов.
Ген: AR, рецептор андрогенов
Полиморфизм: STR (CAG)n (полиморфизм коротких повторяющихся последовательностей).
Рецептор андрогена связывает биологически активный андроген — дигидротестостерон. При связывании рецептора с дигидротестостероном включается цепь биохимических реакций, связанных с эффектами тестостерона в андроген-зависимых тканях. Активность гена AR зависит от длины трехнуклеотидного повтора (CAG)n. От этой активности зависит и баланс между андрогенами и эстрогенами, а также активация генов, регулирующих клеточный цикл. Показана связь между гиперандрогенией, ассоциированной с синдромом поликистозных яичников, и длиной полиморфного участка (CAG)n в гене AR.
40.132 Анализ полиморфизмов в генах 5а-редуктаза, SHBG, AR,CYP17 (кодирующих ферменты метаболизма половых гормонов).
За генный полиморфизм приходится платить
Генные полиморфизмы являются не только источником биоразнообразия и эволюционного материала, но также причиной многих заболеваний человека
Автор
Редакторы
Статья на конкурс «био/мол/текст»: В меняющихся условиях окружающей среды генетическое разнообразие в популяции дает отдельным особям преимущество. Оно не только позволяет виду выживать и существовать в геологических масштабах времени, но и является основой генетической изменчивости и непрерывного процесса видообразования. Обычно белки, кодируемые разными аллелями одного гена, обладают одинаковыми функциональными свойствами, и само по себе наличие генных полиморфизмов не оказывает никакого влияния на жизнедеятельность организма, являясь выражением его биологической индивидуальности. Но эти генетические различия вносят важный вклад в индивидуальные особенности развития защитных реакций и предрасположенность к целому ряду заболеваний, среди которых — невынашивание беременности.
Конкурс «био/мол/текст»-2013
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2013 в номинации «Своя работа».
Спонсор конкурса — дальновидная компания Thermo Fisher Scientific. Спонсор приза зрительских симпатий — фирма Helicon.
Генетическое разнообразие — добро или зло?
Бурное развитие геномики, происходящее в последнее время [1], предоставляет новые мощные инструменты описания и анализа генетического разнообразия. Как правило, гены представлены в популяции двумя или более вариантами — аллелями, — отличающимися между собой либо одиночными заменами нуклеотидов (SNP — single nucleotide polymorphism), то есть реальными изменениями «генетического кода», либо числом повторяющихся фрагментов ДНК. Именно SNP особенно важны для молекулярной диагностики болезней.
Что нового в понимании генетической вариабельности человека и в приложении к персонифицированной медицине дают персональные геномы? Во-первых, открываются новые генетические варианты — в каждом человеческом геноме обнаруживается порядка 3 млн. SNP на 3 млрд. нуклеотидов (это примерный размер генома целиком), что дает уровень различий один нуклеотид на 1000 п.н. Геномы двух разных людей пересекаются примерно по половине SNP. Иногда замена всего одного нуклеотида может стать причиной заболевания, но чаще всего сочетание нескольких генетических полиморфизмов может либо предрасполагать, либо препятствовать проявлению различных заболеваний, и тогда из называют мультифакториальными (МФЗ).
К мультифакториальным заболеваниям относится подавляющее большинство хронических болезней человека, включая сердечнососудистые, эндокринные, иммунные, нервно-психические, онкологические и др. Полиморфизмы «генов предрасположенности» в сочетании с неблагоприятными внешними факторами (нерациональное питание, вредные привычки, загрязнения окружающей среды, инфекции) повышают риск развития заболевания.
В ходе эволюции SNP появляются в результате мутации единого аллеля-предшественника. Такое огромное количество изменений в жизненно-важной генетической программе возникает потому, что в ДНК любой клетки человека ежедневно происходят тысячи случайных изменений (например, депуринизация — отрыв основания аденина или гуанина от нуклеотида), а в процессе репликации самым частым классом ошибок являются замены одиночных пар нуклеотидов. Замена нуклеотида в последовательности ДНК может произойти в регулирующей области гена и значительно изменить уровень его экспрессии (количество транскрибируемой РНК), либо в кодирующей области, отвечающей непосредственно за «считываемый» с гена белок-продукт. А может быть и такой случай, что ДНК мутирует, а продукт гена остается неизменным — в этом случае говорят о синонимичной замене.
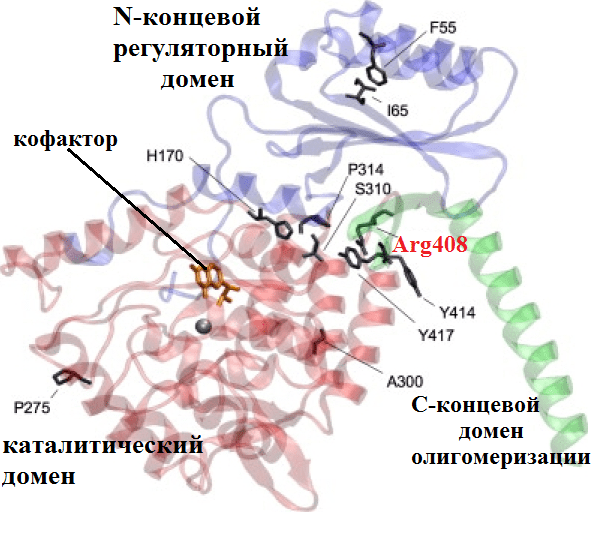
Скорость мутации нуклеотидной пары равна примерно 10 −8 на поколение. Зная число пар нуклеотидов в геноме (3 млрд) можно вычислить, что каждая гамета содержит примерно 30 однонуклеотидных замен, т.е. каждый ребенок в мире рождается с примерно 60 новыми SNP! Изменение одной «буквы» в гене может существенно повлиять на работу белка-продукта за счет изменения пространственной организации белковых доменов (рис. 1), либо за счет нарушения посттранскрипционных изменений РНК (сплайсинга и редактирования) или посттрансляционных модификаций белка (процессинга и присоединения различных химических групп к аминокислотным остаткам). А может и не повлиять. Такие несинонимичные замены (nSNVs — nonsynonymous single nucleotide variants) с точки зрения эволюции считаются нейтральными (ни вредными, ни полезными). Большая часть SNP, конечно же, относится именно к этому классу, иначе рождаемые дети просто-напросто не выживали бы.
Рисунок 1. Вредные несинонимичные замены. Пример такой замены — полиморфизм PAH R408W, причина довольно известного заболевания фенилкетонурии (ФКУ). На этикетках газированных напитков и жевательных резинок можно встретить надпись «не рекомендовано больным фенилкетонурией». А все потому, что эти продукты содержит подсластитель аспартам, который состоит из двух аминокислот — аспарагиновой кислоты и фенилаланина. Организм здорового человека последнюю перерабатывает, однако у больных ФКУ — редким врожденным заболеванием (оно диагностируется у одного из 10 000 новорожденных) — фенилаланин и продукты его распада накапливаются в организме и могут привести к поражению мозга. Больных детей до совершеннолетия нужно кормить пищей, не содержащей фенилаланина. На молекулярном уровне это объясняется тем, что в гене фенилаланин-4-гидроксилазы в 12-м экзоне происходит замена цитозина на тимин. Вследствие этого возникает замена аргинина на триптофан в 408 положении аминокислотной последовательности печеночного фермента, который в норме катализирует превращение фенилаланина в тирозин. В результате замены нарушается сборка активного белка («портится» взаимодействие между двумя субъединицами тетрамера), и фермент не может больше выполнять свои функции. На рисунке изображена доменная структура олигомера гидроксилазы и обнаруженные SNP, нарушающие фолдинг белка [1].
Один ген может иметь много полиморфных вариантов. Большинство замен в них является безвредными (нейтральными). Наиболее часто встречаемый аллель называют нормальным, а редкие варианты — мутантными. Если при конкретном заболевании наблюдается более высокая частота определенного аллельного варианта (неважно — мутантного или нормального), то такой SNP называют ассоциированным с заболеванием, а полиморфный ген — геном-кандидатом предрасположенности к развитию МФЗ. Развитие МФЗ может быть запущено либо одной причиной, либо комбинацией нескольких, которые могут быть чисто генетическими (например, один или несколько аллельных вариантов комплекса генов), либо чисто средовыми (например, химические аллергены, действию которых подвергается работник лакокрасочного завода или парикмахер), либо поведенческими (например, пристрастие к определенной пище), либо социальными или психологическими. При этом индивидуальный вклад каждой причины в проявление болезни может быть незначительным, и только их сумма ведет к развитию заболевания.
Пример МФЗ, к развитию которого приводит только наличие определенных комбинаций аллельных вариантов в генах предрасположенности — невынашивание беременности (НБ) (рис. 2). Сочетание аллельных вариантов с действием факторов среды пока мало изучено, однако на данный момент в мире исследованы SNP более 90 генов, относящихся к генной сети патологии беременности. Большая часть работ посвящена исследованию генов системы детоксикации, фолатного обмена, факторов свертывания крови, HLA-системы, факторов роста, генов антиоксидантной защиты и генов, вовлеченных в воспалительные процессы.
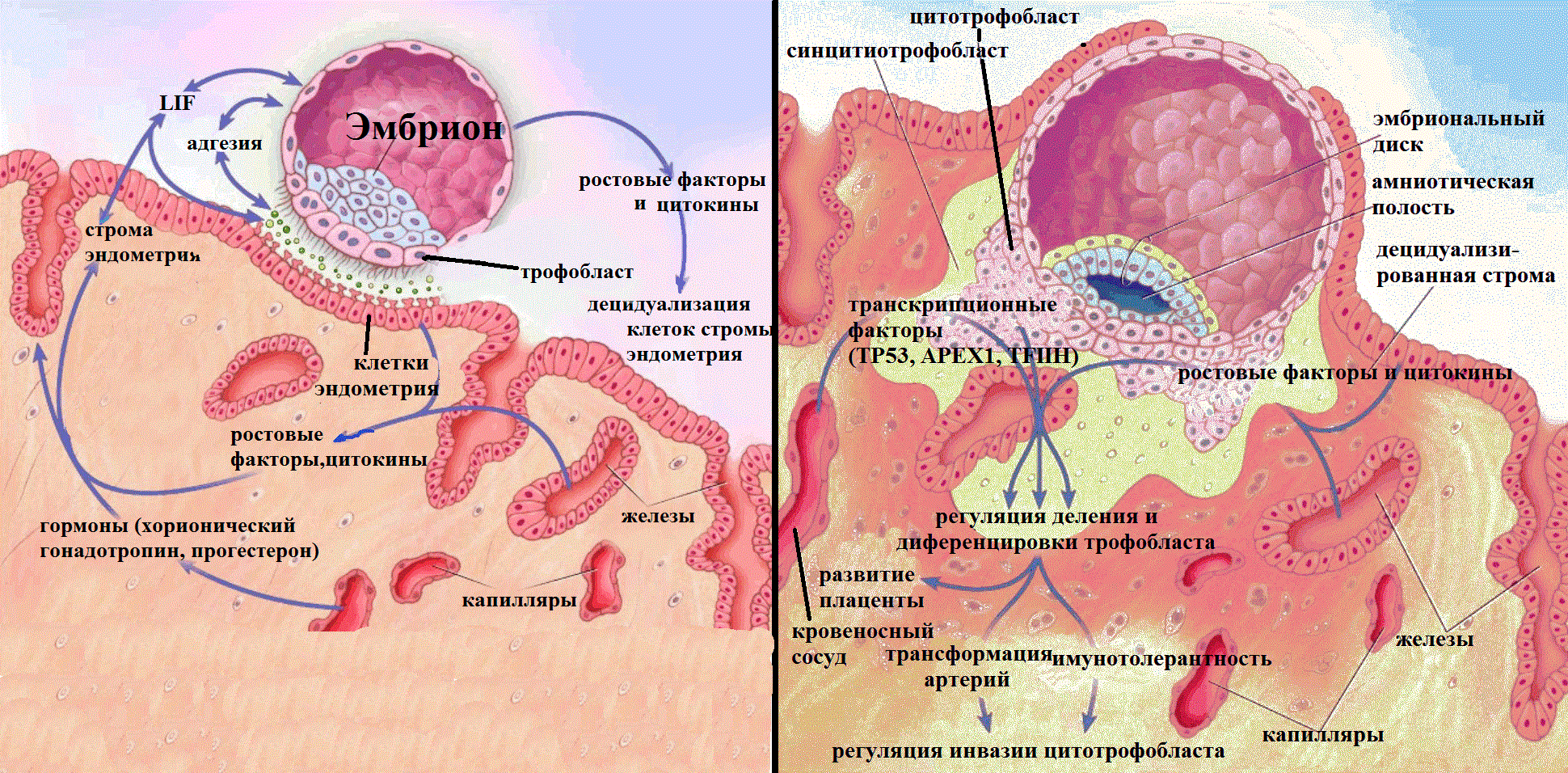
Рисунок 2. Имплантация эмбриона и причины невынашивания. Успех беременности зависит от полноценной имплантации эмбриона в организм матери. Успешная имплантация — результат сложных взаимодействий между гормонально подготовленным эндометрием матки и зрелой бластоцистой. Имплантация бластоцисты в эндометрий включает два этапа: 1) адгезия двух клеточных систем — эндометрия и трофобласта — и 2) децидуализация стромы эндометрия. Затем начинается фаза внедрения трофобласта в стенку эндометрия и активная дифференцировка трофобласта. Активно делящиеся клетки цитотрофобласта, сливаясь, образуют путем эндоредупликации синцитиотрофобласт, напрямую контактирующий с материнской кровеносной системой. В этом процессе активно задействованы все молекулы-участники регуляции и контроля клеточного цикла. Цитотрофобласт внедряется в децидуа и изменяет кровеносные сосуды матери для обеспечения тока крови к плоду: образуются хорион и плацента. Если при формировании плаценты инвазия трофобласта будет недостаточной, то произойдет выкидыш или задержка развития плода [7].
На базе кафедры генетики и НИИ Биологии ЮФУ мы изучали ассоциацию SNP генов, отвечающих за контроль повреждений ДНК, c невынашиванием беременности [5]. Эти гены называются DDR — DNA damage response, — куда относятся гены системы репарации и контроля клеточного цикла, о которых более подробно будет сказано позже.
Большие перемены — результат накопления небольших изменений
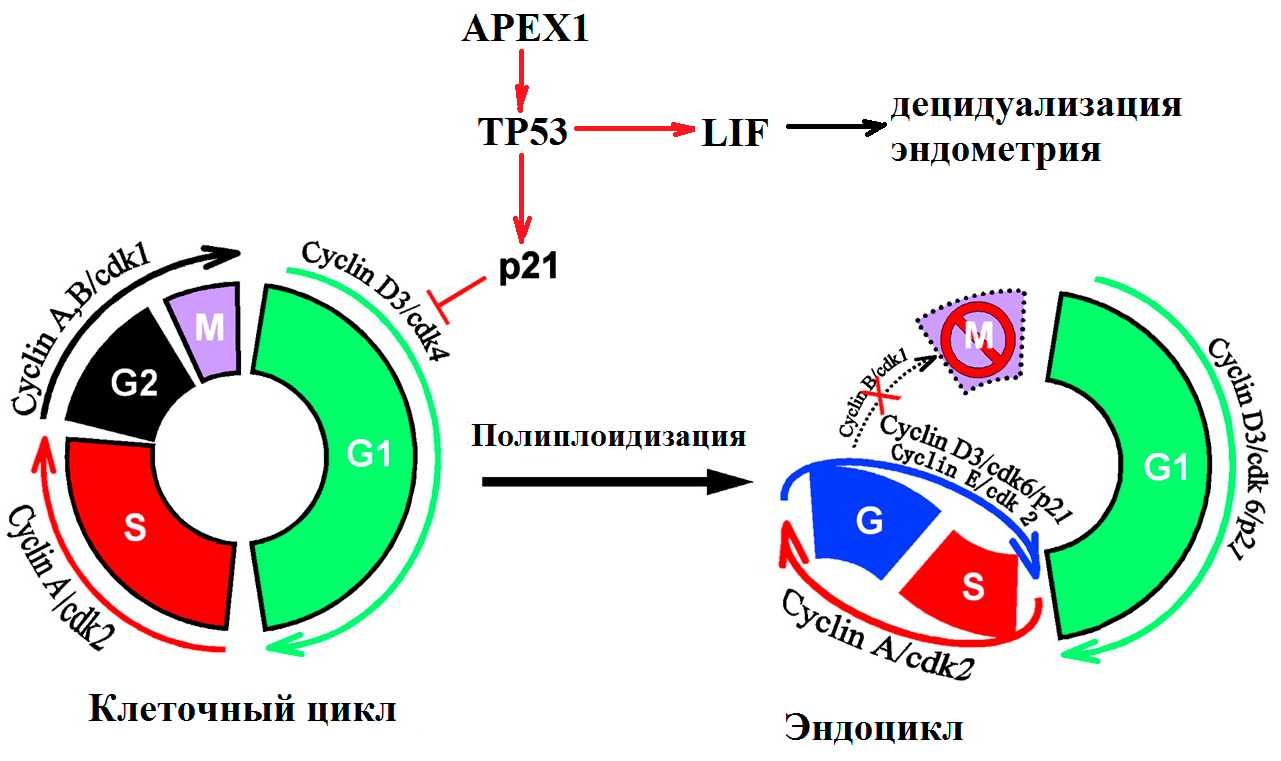
Почему именно эти гены были выбраны для исследования? Все объясняется тем, что в начале развития эмбрион должен внедриться в стенку матки. Это ключевой момент для успешного протекания беременности. При этом клетки трофобласта и стромы эндометрия делятся не традиционным образом, а путем эндоредупликации (удвоения хромосом без деления), невозможной без участия белков, контролирующих клеточный цикл и репарацию (рис. 3).
Рисунок 3. Участие генов системы репарации и контроля клеточного цикла в подготовке к имплантации эмбриона. Процесс образования специализированных клеток децидуа — ключевой для развития беременности. В начале децидуализации стромальные клетки, непосредственно окружающие имплантируемую бластоцисту, активно делятся. Клеточный цикл осуществляется за счет работы циклин-зависимых киназ. Во время деления клеток эндометрия белок p21 подавляет работу комплекса циклина D и киназы cdk4, что приводит к образованию эндоцикла (удвоению хромосом без деления). В результате эндоредупликации получаются гигантские полиплоидные клетки децидуа (до 64n). На рисунке показана роль регуляторов клеточного цикла в «обычном» митозе и в эндоцикле клеток стромы эндометрия и трофобласта [8–10].
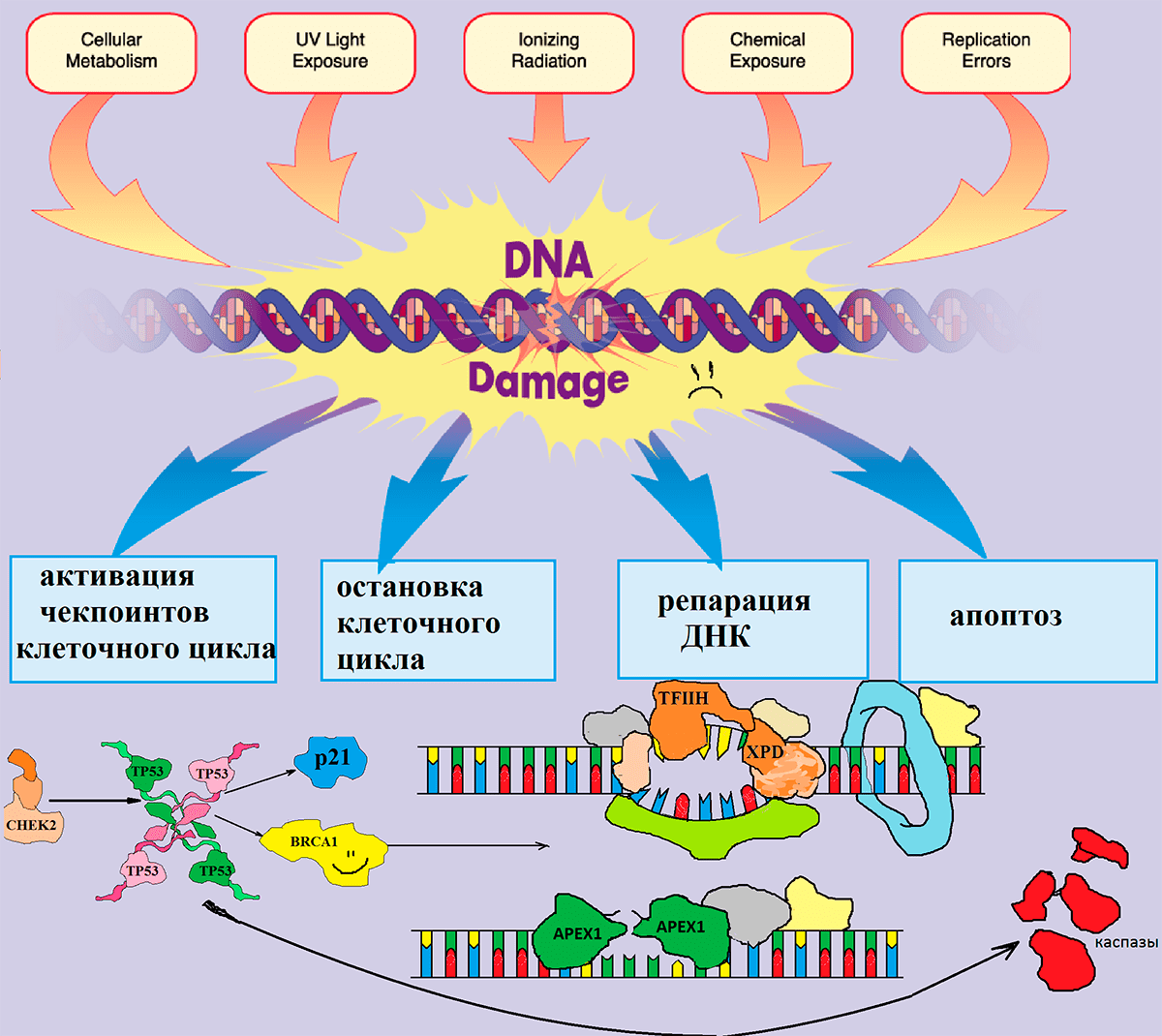
Несмотря на то, что под воздействием неблагоприятных факторов внешней среды, а также во время процесса эндоредупликации происходит огромное количество ошибок, за год в каждой клетке накапливается очень небольшое число стабильных изменений нуклеотидной последовательности. Среди множества случайных замен оснований в ДНК лишь одна на тысячу приводит к возникновению мутации. Все остальные повреждения очень эффективно ликвидируются в процессе репарации ДНК (рис. 4).
Рисунок 4. Механизм работы системы контроля повреждений ДНК. В раннем эмбриональном периоде происходит активное деление как клеток плода, так и материнских клеток. Этот процесс осуществляется ансамблем слаженно действующей системы репарации. Излучения (радиация, УФ), побочные продукты метаболизма, которые образуются внутри клеток, токсины, попадающие в организм с воздухом, пищей или питьем, а также ошибки репликации вызывают изменения в нуклеотидной последовательности ДНК, которые в норме узнаются белками-участниками контроля клеточного цикла.
Среди последних — белковые продукты генов CHEK2 и TP53, которые останавливают деление клеток и являются объектом нашего исследования. После того, как они срабатывают, ошибка исправляется белками репарации, в числе которых — белковые продукты генов APEX1 и XPD, также ставшие объектами нашей работы. Если же ошибку исправить не удастся, то включается механизм «самоубийства» клетки (апоптоза). Всё это вместе составляет сложную сеть взаимодействующих сигнальных каскадов в клетке, изменение работы одного из которых может привести к нарушению работы и гибели клетки.
Показано, что при различных осложнениях беременности наблюдается повышенный уровень апоптоза в трофобласте [4]. В результате происходит недостаточная подготовка стенок матки к имплантации эмбриона и изменения в маточно-плацентарных артериях, что приводит к снижению кровотока в них. Следствием этого является гипоксия, запускающая механизм окислительного стресса. Гипоксия усиливает апоптоз в трофобласте путем повышения экспрессии ТР53.
Именно поэтому для своих исследований мы выбрали гены системы репарации и контроля клеточного цикла. Исследование генов, контролирующих процесс репарации, — одна из важных задач в раскрытии патогенетических звеньев имплантации эмбриона и децидуализации эндометрия. Знание их роли в патогенезе невынашивания беременности позволяет, с одной стороны, прогнозировать риск развития патологии или тяжесть ее течения, с другой — индивидуально подобрать специфическую терапию для конкретного пациента.
История одного исследования
Участницы нашего исследования были разделены на две группы: женщины с нормально протекавшей беременностью, решившие прервать данную беременность на сроке 6–12 недель, и женщины с НБ. Из тканей матери (периферическая кровь и эндометрий) и плода (хорион, эмбрион) выделяли ДНК и изучали геном испытуемых на наличие аллельных вариантов Asp148Glu, Lys751Gln, 1100delC и Pro72Arg генов APEX1, XPD, CHEK2 и TP53, соответственно. Всё это — гены системы контроля клеточного цикла и репарации ДНК.
Анализ экспрессии этих генов позволил выявить возможные причины и механизмы нарушения процессов эмбриогенеза, приводящих к развитию патологии беременности. В ходе исследования мы обнаружили, что при одновременном наличии полиморфных аллелей изучаемых генов (как в генотипе плода, так и в генотипе матери) достоверно повышается вероятность развития патологии беременности. Большая часть полученных нами отличий в частоте полиморфных аллелей между исследуемыми группами выявлена именно при анализе фетальной ткани (хорион), что говорит о значительном вкладе отцовского генотипа в нормальное развитие беременности.
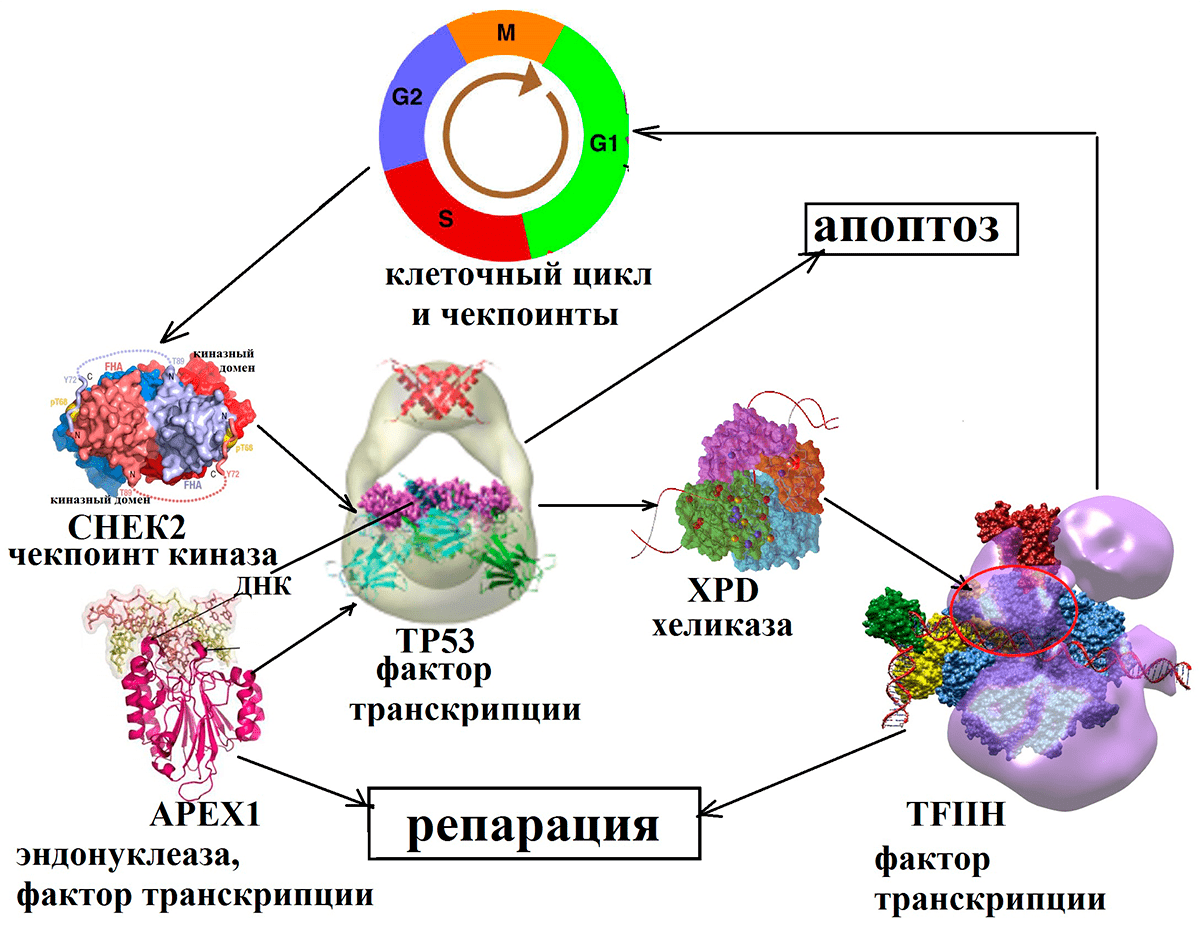
Это объясняется тем, что процесс имплантации эмбриона контролируется сложной молекулярной машиной, руководимой белками-участниками систем репарации и контроля клеточного цикла (рис. 5). Во время активного деления клеток неизбежно возникновение ошибок. Эти ошибки контролируются в специальных «сверочных точках» (чекпоинтах) клеточного цикла. Белки-сенсоры обнаруживают повреждения ДНК и активируют белки-датчики, которые, в свою очередь, активируют белки-эффекторы. Одним из таких белков является CHEK2 (чекпоинт-киназа2). Киназа активирует опухолевый супрессор TP53, известный также как «страж генома». Этот белок подавляет развитие многих типов новообразований, стимулирует остановку клеточного цикла и репарацию или апоптоз (в зависимости от физиологических условий и типа клеток). Действуя в качестве транскрипционного фактора, TP53 связывается со специфическими последовательностями ДНК и активирует большое число генов-мишеней. Известно, например, что TP53 избирательно индуцирует экспрессию гена хорионического гонадотропина человека (ХГЧ). ХГЧ — один из самых ранних формируемых эмбрионом сигналов, который обеспечивает поддержание продукции прогестерона и иммунную толерантность материнских тканей к ткани плода (являющейся наполовину чужеродной для организма матери из-за наличия отцовского генома).
ТР53 вызывает остановку клеточного цикла, активирует репарацию и транскрипцию необходимых для этого процесса генов (XPD, APEX1). APEX1 — эндонуклеаза, разрезающая ДНК в депуринизованных участках, способствуя процессам репарации. Кроме того, она может выступать в качестве транскрипционного фактора, активирующего ТР53 в ответ на окислительный стресс. Ген XPD кодирует белок, носящий название «хеликазная XPD субъединица основного комплекса транскрипционного фактора TFIIH». (Хеликаза — это белок, «расплетающий» двойную спираль во время репликации.) В случае успешной репарации ход клеточного цикла возобновляется, в противном же случае ТР53 запускает механизм апоптоза.
Рисунок 5. Взаимодействие белков репарации и контроля клеточного цикла. В ответ на повреждение ДНК чекпоинт-киназа активирует опухолевый супрессор, который вызывает остановку клеточного цикла и активирует хеликазу и эндонуклеазу, осуществляющие репарацию.
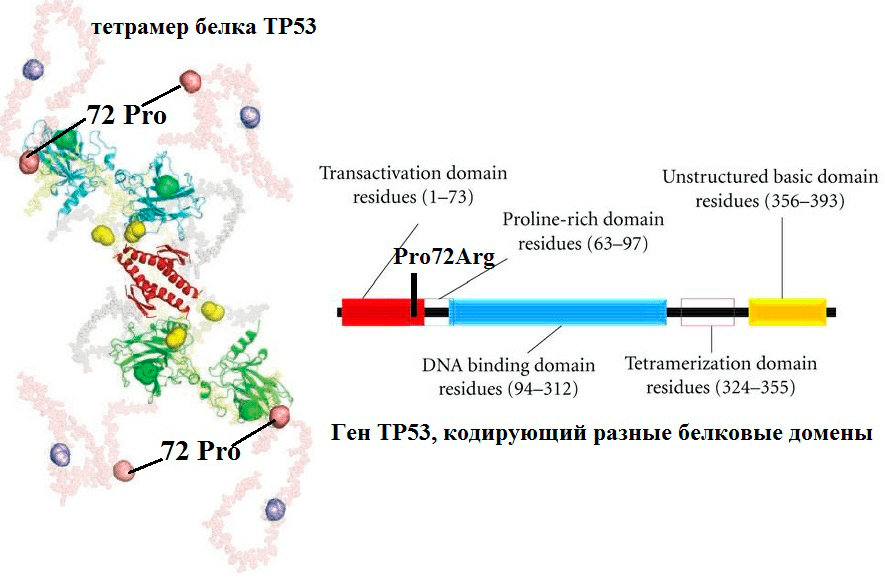
В результате SNP гена в молекуле его белкового продукта одна аминокислота может быть заменена на другую, что приводит к изменению конформации, размера, заряда и других свойств белка. Часто эти изменения приводят к изменению активности (как в случае с TP53, рис. 6) или потере функции (как в случае с CHEK2, рис. 7).
Рисунок 6. Повышение активности белка опухолевого супрессора TP53 в результате SNP кодирующего его гена. Полиморфизм Pro72Arg белка TP53 расположен в участке, богатом пролином и отвечающем за взаимодействие ингибитором TP53. Ингибитор связывается с Pro-формой гораздо сильнее, чем с Arg-формой, поэтому TP53/Arg72 эффективнее активирует апоптоз, чем исходная форма.
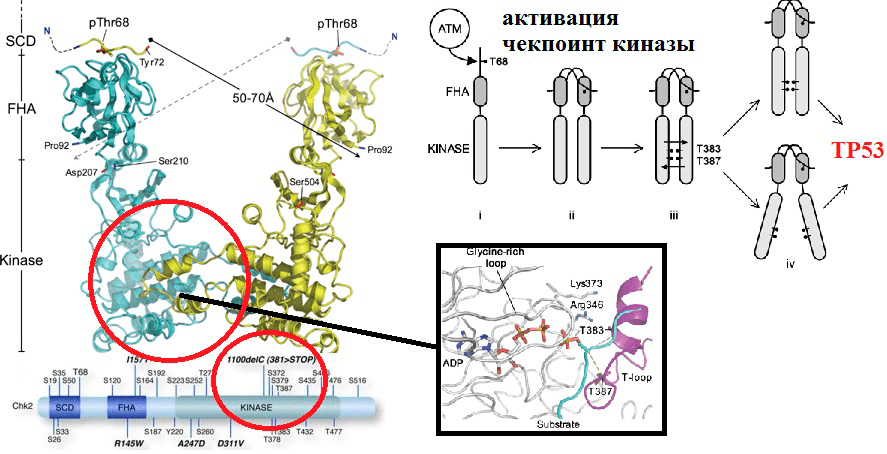
Рисунок 7. Потеря белком киназной функции в результате SNP в кодирующем его гене. Полиморфизм 1100delC гена CHEK2 приводит к экспрессии укороченного киназного домена. Это приводит к тому, что активация белка в ответ на повреждения ДНК становится невозможной (для нее необходимы 387 и 383 остатки треонина, а длина мутантного белка лишь 381 остаток из-за делеции).
При случайном одновременном наличии нескольких аллельных вариантов, продукты генов которых задействованы в выполнении схожих функций, может произойти нарушение работы всего метаболического пути и клетки в целом. Так, полиморфизм Lys751Gln гена XPD нарушает связывание с транскрипционным фактором (ТФ) IIH, действующим на ядерные рецепторы и обеспечивающим контроль активации генов гормонального ответа, необходимый для нормального развития плаценты. Вследствие этого в сыворотке крови матери повышается уровень ХГЧ (хорионического гонадотропина человека) и нарушается функция плаценты. SNP попадает в домен, богатый пролином, необходимый белку для полной индукции апоптоза. В случае неэффективной имплантации эмбриона и возникновения гипоксии будут нарушены механизмы апоптоза. Кроме того, ТР53 не сможет эффективно активировать необходимый для имплантации регулятор LIF и белок р21, запускающий процесс эндоредупликации в эндометрии, а также ХГЧ, участвующий в плацентации посредством стимуляции роста сосудов.
Полиморфные варианты генов системы репарации и контроля клеточного цикла производят менее активные белки репарации и специфические протеинкиназы, что вносит немалый вклад в развитие патологии беременности вследствие несрабатывания механизма корректировки повреждений ДНК, появления геномной нестабильности и запуска апоптоза в материнских и фетальных клетках (клетках плода), что подтвердилось в ходе нашего исследования.
По ту сторону добра и зла
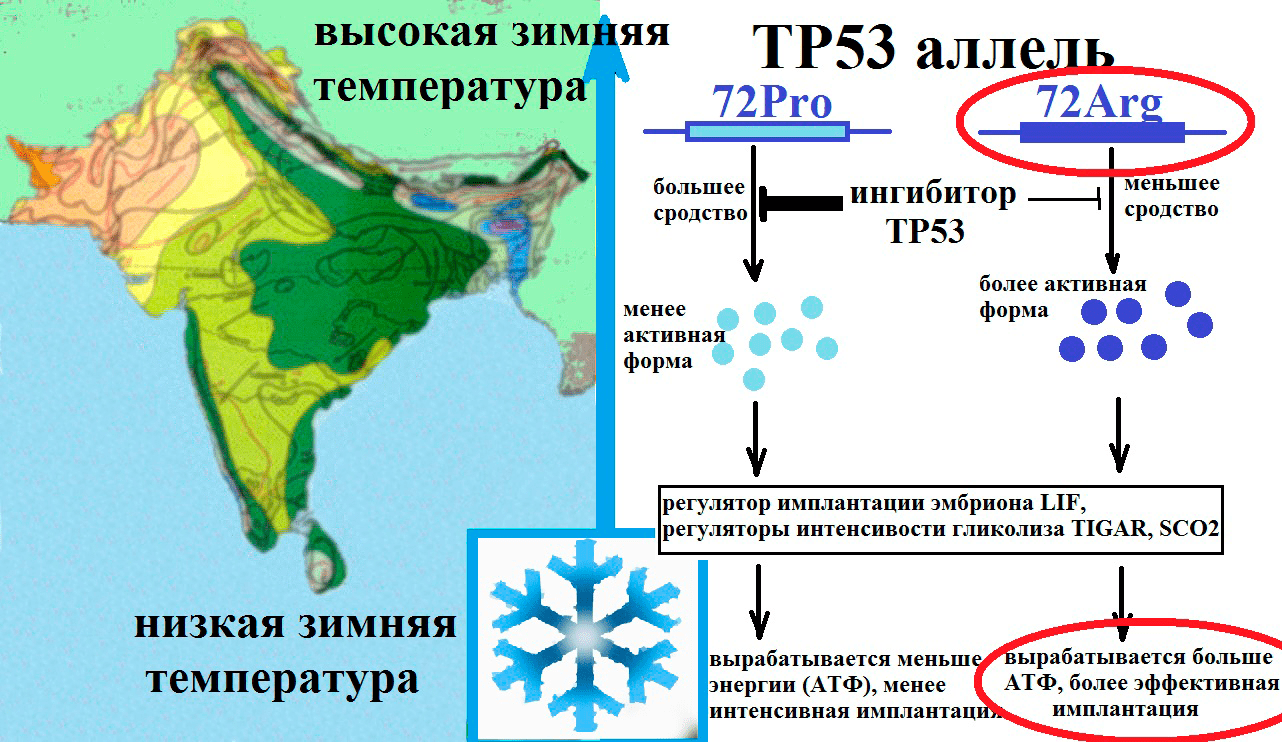
Особенности спектров генетических полиморфизмов в зависимости от географических условий, диеты и этнической принадлежности говорят о невидимой руке естественного отбора. Имеются исследования, в которых было установлено, что частота аллеля Pro гена ТР53 тесно связана с географической широтой и температурой: она гораздо выше в экваториальных популяциях (рис. 8) [6].
Рисунок 8. Предполагаемый механизм отбора полиморфизма гена TP53. Под влиянием более низких температур в популяции отбирается TP53 Arg72 аллель, так как он дает более активную форму TP53, повышающего активность белков SCO2 (участвует в синтезе АТФ) и TIGAR (участвует в регуляции гликолиза и защите от окислительного стресса). TP53 Arg72 аллель участвует в регуляции метаболизма и имплантации эмбриона и повышении уровня приспособленности.
Эти факты особенно интересны в свете нейтральной теории молекулярной эволюции (НТМЭ), которая объясняет происхождение и распределение nSNV, ассоциированных с болезнями. Авторы одного из недавних исследований предполагают, что большинство аллельных вариантов, ассоциированных с заболеваниями, в современных человеческих популяциях изначально были нейтральными, а некоторые из них могли иметь адаптивное значение (например, замена глутамина на валин в одной из цепей гемоглобина — причина серповидно-клеточной анемии). В рамках этой теории nSNV, ассоциированные с МФЗ, имеют равную скорость эволюции с нейтральными nSNV. Это объясняется тем, что на них, в отличие от nSNV, приводящих к развитию моногенных болезней (например, фенилкетонурии), не действует очищающий отбор, элиминирующий заболевших индивидов [3]. Этот подход хорошо объясняет то, что исследуемый нами полиморфизм Asp148Glu гена АРЕХ1 является исключительно нейтральным для функционирования белка — он не теряет своей эндонуклеазной активности [11], — однако нами выявлена достоверная связь между наличием этого SNP в генотипе матери или плода и невынашиванием беременности.
Таким образом, НТМЭ обеспечивает клиническую генетику информативной базой для объективной оценки адаптивных событий человеческой истории как одной из основных причин заболеваний человека.
Заключение
Индивидуальный вклад каждой причины в проявление болезни может быть незначительным, и только их суммы может оказаться достаточно для развития заболевания. Именно поэтому очень сложно определить, какой именно фактор послужил сигналом для запуска патогенеза. С точки зрения индивидуального прогноза здоровья и оценки риска МФЗ каждый персональный геном дает исчерпывающую информацию о носительстве аллелей, связанных с клиническими фенотипами. Ярким примером МФЗ является невынашивание беременности (НБ). Частота невынашивания в первые три месяца беременности может достигать 80%, и, по меньшей мере, половина этих случаев происходит по непонятным причинам.
Интеграция геномики и феномики в рамках системной биологии, появившиеся в последнее время новые мощные инструменты описания и анализа генетического разнообразия — секвенирование индивидуальных геномов [12] и полногеномный анализ SNP на биочипах, проекты HapMap и «1000 геномов» [1] — дают надежду на быстрый прогресс в каталогизации генетического разнообразия, связанного с риском развития распространенных болезней. Эта информация повысит эффективность лекарственной терапии и перебросит мостик от фундаментальных научных исследований к доказательным рекомендациям в персонифицированной медицине.
Молекулярно-генетическая диагностика позволит врачу заглянуть в индивидуальную программу жизни человека, увидеть особенности его организма, предрасположенность к одним заболеваниям и устойчивость к другим. Таким образом, диагностика заболеваний на досимптомном этапе развития [13] позволит своевременно провести адекватную профилактику заболевания (например, невынашивания беременности или сахарного диабета) и назначить индивидуальную, подходящую именно для этого пациента схему лечения.
Существование генных полиморфизмов является результатом действия факторов микроэволюции и вносит вклад в генетическое разнообразие популяции, тем самым обеспечивая их удивительной способностью изменяться в соответствии с бесконечной изменчивостью окружающего мира. Исследование и выявление генных полиморфизмов, вносящих вклад в развитие того или иного заболевания, имеет прямую прогностическую ценность. Именно такой подход к терапии позволит свести к минимуму неблагоприятные эффекты лекарственных препаратов, сохранить пациенту здоровье и даже жизнь.